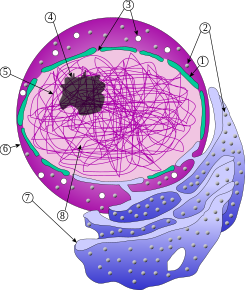
Nucleu celular
En bioloxía, el nucleu celular ye un orgánulo membranosu'l cual atópase nel centru de les célules eucariotes. Contién la mayor parte del material xenético celular, entamáu en múltiples molécules lliniales d'ADN de gran llargor, formando complexos con una gran variedá de proteínes como les histones pa formar los cromosomes. El conxuntu de xenes d'esos cromosomes denominar xenoma nuclear. La función del nucleu ye caltener la integridá d'esos xenes y controlar les actividaes celulares regulando la espresión xénica. Por ello dizse que'l nucleu ye'l centru de control de la célula.
| Nucleu celular | ||
|---|---|---|
|
1. Envoltura nuclear | ||
| Llatín | Nucleus | |
| TH | H1.00.01.0.00003 | |
| [editar datos en Wikidata] | ||

La principal estructura que constitúi'l nucleu ye la envoltura nuclear, una doble membrana qu'arrodia dafechu al orgánulo y dixebra esi conteníu del citoplasma, amás de cuntar con poros nucleares que dexen el pasu al traviés de la membrana pa la espresión xenética y el caltenimientu cromosómico.
Anque l'interior del nucleu nun contién nengún subcompartimento membranosu, el so conteníu nun ye uniforme, esistiendo una cierta cantidá de cuerpos subnucleares compuestos por tipos esclusivos de proteínes, molécules d'ARN y segmentos particulares de los cromosomes. El meyor conocíu de toos ellos ye'l nucléolo, que principalmente ta implicáu na síntesis de los ribosomes. En siendo producíos nel nucléolo, éstos espórtense a la citoplasma, onde traducen l'ARNm.
Historia
editarEl nucleu foi'l primer orgánulo en ser descubiertu. Probablemente, el dibuxu más antiguu que se caltién d'esti orgánulo remontar a unu de los primeros microscopistas, Anton van Leeuwenhoek (1632–1723). Esti investigador reparó un buecu o "lumen", el nucleu, n'eritrocitos de salmón.[1] Al contrariu que los eritrocitos de mamíferu, los del restu de vertebraos son nucleados. El nucleu tamién foi descritu en 1804 por Franz Bauer, y darréu con más detalle pol botánicu escocés Robert Brown nuna charra dictada ante la Sociedá linneana de Londres en 1831.[2] Brown taba estudiando la estructura microscópica de les orquídees cuando reparó una área opaca, que llamó areola o nucleu, nes célules de la capa esterna de la flor, magar nun suxurió una función potencial pa tal estructura.[3] En 1838 Matthias Schleiden propunxo que'l nucleu desempeñaba un papel na xeneración de célules, denominándolo por ello "citoblasto" (constructor de célules). Pensaba que reparara célules nueves alredor d'estos "citoblastos". Franz Meyen foi un fuerte opositor d'esta opinión describiendo primeramente célules que se multiplicaben por división y creyendo que munches célules escareceríen de nucleu. La idea de que les célules podíen xenerase de novo, bien pol "citoblasto" o bien d'otra miente, contradicía los trabayos de Robert Remak (1852) y Rudolf Virchow (1855) quien arrobinaron decisivamente el nuevu paradigma de que les célules solo yeren xeneraes por otres célules ("Omnis cellula y cellula"). La función del nucleu permanecía ensin esclariar.[4]
Ente 1876 y 1878 Oscar Hertwig publicó dellos estudios sobre la fecundación de güevos d'oriciu, amosando que'l nucleu del espermatozoide entraba nel oocito, fundiéndose col so nucleu. Esta foi la primer vegada que se suxurió qu'un individuu desenvolver a partir d'una sola célula nucleada. Esto taba en contradicción cola teoría d'Ernst Haeckel qu'enunciaba que se repitía la filoxenia completa d'una especie mientres el desenvolvimientu embrionariu, incluyendo la xeneración de la primer célula nucleada a partir d'una "monerula", una masa desestructurada de mocu primordial ("Urschleim", n'alemán). Poro, la necesidá del nucleu espermático pa la fecundación tuvo en discutiniu por un tiempu. Sicasí, Hertwig confirmó la so observación n'otros grupos animales, como por casu n'anfibios y moluscos. Eduard Strasburger llogró les mesmes resultancies en plantes (1884). Esto allanó el camín pa la asignación d'un papel importante del nucleu na heriedu. En 1873 August Weismann postuló la equivalencia de les célules xerminales paternes y maternes nel heriedu. La función del nucleu como portador d'información xenética fíxose patente solo dempués, tres el descubrimientu de la mitosis y el redescubrimientu de la heriedu mendeliana a principios del sieglu XX. Esto supunxo'l desenvolvimientu de la teoría cromosómica del heriedu.[4]
Estructures
editarEl nucleu ye'l orgánulo de mayor tamañu nes célules animales.[5] Nes célules de mamíferu, el diámetru permediu del nucleu ye d'aproximao 6 micrómetros (μm), lo cual ocupa aproximao'l 10 % del total del volume celular.[6] Nos vexetales, el nucleu xeneralmente presenta ente 5 a 25 µm y ye visible con microscopiu ópticu. Nos fungos reparáronse casos d'especies con nucleos bien pequeños, d'alredor de 0,5 µm, que son visibles solamente con microscopiu electrónicu. Nes oósferas de Cycas y de coníferes algama un tamañu de 0,6 mm, ye dicir que resulta visible a güeyu.[7]
El líquidu mafoso del so interior denominar nucleoplasma y la so composición ye similar a la que s'atopa nel citosol del esterior del nucleu.[8] A les traces tien l'aspeutu d'un orgánulo trupu y esféricu.
Envoltura y poros nucleares
editarLa envoltura nuclear, ye dacuando llamada membrana nuclear indebidamente, porque se compón de, ente otres coses, dos membranes, una interna y otra esterna, dispuestes en paralelu una sobre la otra. Atópase furada por poros, gracies a estos poros nucleares esiste un movimientu bidireccional establecíu ente'l citosol de la célula y el nucleu. Evita que les macromolécules espublicen llibremente ente'l nucleoplasma y la citoplasma.[9] La membrana nuclear esterna ye continua cola membrana del retículo endoplásmico rugoso (RER), y ta igualmente llarada de ribosomes. L'espaciu ente les membranes conozse como espaciu o cisterna perinuclear y ye continuu cola lluz del RER.
Los poros nucleares, qu'apurren canales aguacientes abiertos polos que pueden espublizar por tresporte pasivu molécules pequeñes (que van de 5000 a 44000 Da) y solubles n'agua, tamién prohibe'l pasu escontra'l nucleu a proteínes globulares mayores de 60kDa. El tamañu de les canales dexa que'l compartimientu nuclear y el citosol caltengan distintos conxuntos de proteínes, tán formaos por subunidades denominaes nucleoporinas (participando alredor de 30 nucleoporinas distintes na formación d'un solu poru nuclear), que de la mesma tán arrexuntaes en sub-complexos multiproteicos allugaos dientro de la envoltura nuclear o acomuñaos a la so cara esterna o interna respectu al nucleoplasma. Los poros tienen 125 millones de daltons de pesu molecular y compónense d'aproximao 50 (en lleldos) a 100 proteínes (en vertebraos).[5] Los poros tienen un diámetru total de 100 nm; sicasí, el buecu pol qu'espublicen llibremente les molécules ye de 9 nm d'anchu por cuenta de la presencia de sistemes de regulación nel centru del poru. Esti tamañu dexa'l llibre pasu de pequeñes molécules hidrosolubles ente qu'evita que molécules de mayor tamañu entren o salgan de manera desaparente, como acedos nucleicos y proteínes grandes. Estes molécules grandes, en llugar d'ello, tienen de ser tresportaes al nucleu de forma activa. El nucleu típicu d'una célula de mamíferu dispón d'ente 3000 y 4000 poros a lo llargo de la so envoltura,[10] cada unu de los cualos contién una estructura n'aniellu con simetría octal na posición na que les membranes, interna y esterna, fúndense.[11] Fondiada al aniellu atopa la estructura denomada cesta nuclear que s'estiende escontra'l nucleoplasma, y una serie d'estensiones filamentosas que se proyeuten na citoplasma. Dambes estructures medien la unión a proteínes de tresporte nucleares.[5]
La mayoría de les proteínes, subunidades del ribosoma y dellos ARNs trespórtense al traviés de los complexos de poru nun procesu mediáu por una familia de factores de tresportes conocíes como carioferines. Ente éstes atopen les importines, qu'intervienen nel tresporte en direición al nucleu, y les que realicen el tresporte en sentíu contrariu, que se conocen como exportines. La mayoría de les carioferinas interactúan direutamente cola so carga, anque dalgunes utilicen proteínes adaptadores.[12] Les hormones esteroideas como'l cortisol y l'aldosterona, según otres molécules pequeñes hidrosolubles implicaes na señalización celular, pueden espublizar al traviés de la membrana celular y na citoplasma, onde se xunen a proteínes qu'actúen como receptores nucleares que son conducíes al nucleu. Sirven como factores de trescripción cuando se xunen a la so amestando. N'ausencia d'amestando munchos d'esti receptores funcionen como histona deacetilasas que reprimen la espresión xénica.[5]
Llámina nuclear
editarNes célules animales esisten dos red de filamentos entemedios qu'apurren soporte mecánicu al nucleu: la llámina nuclear forma una trama entamada na cara interna de la envoltura, ente que na cara esterna esti soporte ye menos entamáu. Dambes redes de filamentos entemedios tamién sirven de llugar de anclaje pa los cromosomes y los poros nucleares.[6]
La llámina nuclear ta compuesta por proteínes que se denominen lamines o proteínes llaminares. Como toles proteínes, éstes son sintetizaes na citoplasma y más tarde trespórtense al interior del nucleu, onde se ensamblan antes d'incorporase a la rede presistente.[13][14] Les laminas tamién s'atopen nel interior del nucleoplasma, onde formen otra estructura regular conocida como velo nucleoplásmico,[15] que ye visible mientres la interfase.[16] Les estructures de les llámines que formen el velu xunir a la cromatina y por aciu la disrupción de la so estructura inhiben la trescripción de xenes que codifican pa proteínes.[17]
Como los componentes d'otros filamentos entemedios, los monómeros de lamina contienen un dominiu alfa helicoidal, utilizáu por dos monómeros pa enroscase l'unu col otru, formando un dímero con un motivu en héliz arrollada. Dos d'eses estructures dimétricas xúnense darréu llau con llau dispuestos de manera antiparalelo pa formar un tetrámeru denomináu protofilamento. Ocho d'esos protofilamentos dispónense lateralmente pa formar un filamentu. Esos filamentos puédense ensamblar o desensamblar de manera dinámica, lo que significa que los cambeos nel llargor del filamentu dependen de les tases en competición de adición y desplazamientu.[6]
Les mutaciones nos xenes de les laminas conducen a defectos nel ensamblaxe de los filamentos conocíes como laminopatíes. D'éstes, la más destacable ye la familia d'enfermedaes conocida como progeries, que dan l'apariencia d'un avieyamientu prematuru a quien la sufren. Desconozse'l mecanismu exactu pol que los cambeos bioquímicos asociaos dan llugar al fenotipu progeroide.[18]
En casu de que la llámina nuclear suma'l nucleu sume, y en casu de volvese a formar el nucleu volverá tar; esta ye una propiedá bien importante especialmente na mitosis.
Cromosomes
editarEl nucleu celular contién la mayor parte del material xenético celular en forma de múltiples molécules lliniales d'ADN conocíes como cromatina, y mientres la división celular ésta apaez na forma bien definida que se conoz como cromosoma. Una pequeña fracción de los xenes asitiar n'otros orgánulos, como les mitocondrias o los cloroplastos de les célules vexetales.
Hai de solliñar que la composición química de la fibra de cromatina anicia en segmentos d'ADN acomuñaos a proteínes histónicas y non histónicas, quien se doblen na fase S de la interfase. Les proteínes histónicas son: H1, H2A, H2B, H3 y H4; dos H2A amiéstense con dos H2B per mediu de la proteína non histónica nucleoplasmina, ente que dos H3 y dos H4 xunir con ayuda de la proteína N1, conformando asina un octámero, que ye arrodiáu per una dos vueltes y media d'ADN pa consolidar nucleosoma. Esti postreru, al tar suxetáu pola H1 pasa a llamase cromatosoma, y ante la proximidá de la fase M estes H1 entren en contautu direutu pa consolidar un solenoide de 30 nm de diámetru.
Esisten dos tipos de cromatina: la eucromatina ye la forma d'ADN menos compacta, y contién xenes que son frecuentemente espresaos pola célula.[19] L'otru tipu, conocíu como heterocromatina, ye la forma más compacta, y contién ADN que se trescribe de forma infrecuente. Esta estructura clasifícase de la mesma en heterocromatina facultativa, que consiste en xenes que tán entamaos como heterocromatina solo en ciertos tipos celulares o en ciertos estadios del desenvolvimientu, y heterocromatina constitutiva, que consiste en componentes estructurales del cromosoma como los telómeros y los centrómeros.[20] Mientres la interfase la cromatina entamar en territorios individuales discretos, los territorios cromosómicos.[21][22] Los xenes activos, que s'atopen xeneralmente na rexón eucromática del cromosoma, tienden a alcontrase nes fronteres de los territorios cromosómicos.[23]
Acomuñáronse anticuerpos a ciertos tipos d'organización cromatínicasobremanera los nucleosomes con delles enfermedaes autoinmunes como'l lupus eritematoso sistémico.[24] Estos son conocíos como anticuerpos antinucleares (ANA) y tamién se repararon en conciertu cola esclerosis múltiple nel contestu d'una disfunción inmune xeneralizada.[25] Como'l casu antes mentáu de la progeria, el papel que desempeñen los anticuerpos na inducción de los síntomes de la enfermedá autoinmune nun ta inda esclariáu.
Nucléolo
editarEl nucléolo ye una estructura discreta que se tiñe densamente y atópase nel nucleu. Nun ta arrodiáu per una membrana, polo que n'ocasiones se diz que ye un suborgánulo. Fórmase alredor de repeticiones en tándem d'ADNr, que ye l'ADN que codifica el ARN ribosómico (ARNr). Estes rexones llámense organizadores nucleolares. El principal papel del nucléolo ye sintetizar el ARNr y ensamblar los ribosomas. La cohesión estructural del nucléolo depende de la so actividá, yá que l'ensamblaxe ribosómico nel nucléolo resulta nuna asociación transitoria de los componentes nucleolares, facilitando'l posterior ensamblaxe d'otros ribosomas. Esti modelu ta sofitáu pola observación de que la inactivación del ARNr da como resultáu na "amiestu" de les estructures nucleolares.[26]
El primer pasu del ensamblaxe ribosómico ye la trescripción del ADNr pola ARN polimerasa I, formando un llargu pre-ARNr precursor. Ésti ye biforcáu nes subunidades 5,8S, 18S, y 28S ARNr.[27] La trescripción, procesamientu post-transcripcional y ensamblaxe del ARNr tien llugar nel nucléolo, ayudáu por molécules d'ARN pequeñu nucleolar, dalgunes de les cualos derívense d'intrones ayustados d'ARN mensaxeru rellacionaos cola función ribosomal. Estes subunidades ribosomales ensambladas son les estructures más grandes que pasen al traviés de los poros nucleares.[5]
Cuando se repara sol microscopiu electrónicu, puede vese que'l nucléolo componer de tres rexones estremables: los centros fibrilares (FCs), arrodiaos pol componente fibrilar mestu (DFC), que de la mesma ta bordiáu pol componente granular (GC). La trescripción del ADNr tien llugar tantu nel FC como na zona de transición FC-DFC, y por ello cuando la trescripción del ADNr aumenta, reparar más FC's. La mayor parte de la dixebra y cambéu de los ARNr tien llugar nel DFC, ente que los últimos pasos qu'impliquen l'ensamblaxe de proteínes nes subunidades ribosómicas tienen llugar nel GC.[27]
Otros cuerpos subnucleares
editar| Nome de la estructura | Diámetru de la estructura |
|---|---|
| Cuerpos de Cajal | 0,2-2,0 µm[28] |
| PIKA | 5 µm[29] |
| Cuerpos PML | 0,2–1,0 µm[30] |
| Paraspeckles | 0,2–1,0 µm[31] |
| Speckles | 20–25 nm[29] |
Amás del nucléolo, el nucleu contién una cierta cantidá de cuerpos delimitados non membranosos. Ente éstos atopen los cuerpos de Cajal (cuerpos endolcaos), los llamaos "Xéminis de los cuerpos endolcaos" (Gemini of coiled bodies, en inglés), la denomada Asociación Cariosómica Polimórfica Interfásica (PIKA, poles sos sigles en inglés de Polymorphic Interphase Karyosomal Association), los Cuerpos de la Leucemia Promielocítica (PMLs, poles sos sigles en inglés de promyelocytic leukaemia), los "paraspeckles" y los "specles de ayuste" o "llixos d'empalme" ("splicing speckles" en inglés). Anque se sabe pocu sobre'l númberu d'estos dominios subnucleares, son significativos en cuantes qu'amuesen que'l nucleoplasma nun ye un amiestu uniforme, sinón que más bien contién subdominios funcionales entamaos.[30]
Otres estructures subnucleares apaecen como parte de procesos patolóxicos. Por casu, viose la presencia de pequeños cayaos intranucleares en dellos casos de miopatía nemalínica. Esta enfermedá produzse típicamente por mutaciones nel xen de l'actina, y los cayaos en sí mesmos tán constituyíos pola actina producida a partir de tales xenes mutantes, según otres proteínes del citoesqueleto.[32]
Cuerpos de Cajal y GEMs
editarEl nucleu típicu tien de 1 a 10 estructures compactes denominaes Cuerpos de Cajal o cuerpos endolcaos (CBs, poles sos sigles en inglés de Coiled Bodies), que'l so diámetru mide ente 0,2 µm y 2,0 µm dependiendo del tipu celular y especie.[28] Cuando se reparen sol microscopiu electrónicu, asemeyar a duviellos de filos enrevesosos,[29] y son focos trupos de distribución de la proteína coilina.[33] Los CBs tán implicaos en dellos tipos distintos de funciones rellacionaes col procesamientu de ARN, específicamente na maduración del ARN nucleolar pequeñu (snoRNA) y el ARN nuclear pequeñu (snRNA), y cambéu del ARNm d'histones.[28]
Asemeyaos a los cuerpos de Cajal atópense los "Xéminis de cuerpos endolcaos o GEMs (poles sos sigles en inglés de Gemini of Coiled Bodies), que'l so nome derivar de la constelación de Xéminis pola so rellación casi como de ximielgos colos Cuerpos de Cajal. Los GEMs son similares en forma y tamañu a éstos últimos, y de fechu son virtualmente indistinguibles al microscopiu.[33] A diferencia de los cuerpos de Cajal, nun contienen snRNPs, pero contienen una proteína que se denomina motoneurona sobreviviente (SMN, poles sos sigles en inglés de survivor of motor neurons), que la so función rellacionar cola bioxénesis del snRNP. Créese que los GEMs ayuden a los CBs na bioxénesis del snRNP,[34] anque tamién se suxurió a partir d'evidencies de microscopía que los CBs y los GEMs son distintes manifestaciones de la mesma estructura.[33]
Dominios PIKA y PTF
editarLos dominios PIKA, o Asociaciones Cariosómicas Polimórficas de Interfase, fueron descritos per primer vegada n'estudios de microscopía en 1991. La so función yera y permanez pocu clara, anque nun se piensa que tean acomuñaos cola replicación activa d'ADN, trescripción o procesamientu de ARN.[35] Viose que frecuentemente s'acomuñar con dominios discretos definíos por llocalizaciones trupes del factor de trescripción PTF, que promueve la trescripción del ARNnp.[36]
Cuerpos PML
editarLos cuerpos PML o de la proteína de la leucemia promielocítica (PML, poles sos sigles en inglés de Promyelocytic leukaemia) son cuerpos esféricos que s'atopen esvalixaos nel nucleoplasma, y que miden alredor de 0,2–1,0 µm. Conocer por otros nomes, como dominiu «nuclear 10» (ND10), «cuerpos de Kremer», y «dominios oncogénicos PML». De cutiu vense nel nucleu acomuñaos colos cuerpos de Cajal. Suxurióse que desempeñen un papel na regulación de la trescripción. Soler identificar en célules tumorales (como en casos de Leucemia promielocítica aguda) polo que tamién actúen como marcadores tumorales.[30]
Paraspeckles
editarDescubiertos en 2002, los paraspeckles son compartimientos de forma irregular del espaciu intercromatínico del nucleu.[37] Fueron documentaos per primer vegada en célules HeLa, onde polo xeneral atopar ente 10–30 por nucleu,[38] anguaño sábese que los paraspeckles tamién esisten en toles célules primaries humanes, los llinaxes de célules tresformaes y les seiciones de texíos.[39] El so nome derivar de la so distribución nel nucleu. El prefixu "pa" ye una apócope de "paralelu" y "speckles" (mancha o llixu, n'inglés) referir a la so proximidá a los "splicing speckles" o llixos de ayuste.[38]
Los paraspeckles son estructures dinámiques que s'alterien en respuesta a cambeos na actividá celular metabólica. Son dependientes de la trescripción,[37] y n'ausencia de trescripción de la ARN Pol II, los paraspeckles sumen, y toles proteínes acomuñar que lo componen (PSP1, p54nrb, PSP2, CFI(m)68 y PSF) formen un tapón perinucleolar en forma de cuartu creciente nel nucléolo. Esti fenómenu manifestar mientres el ciclu celular, nel que tán presentes en interfase y mientres tola mitosis, sacante en telofase. Mientres la telofase, cuando los dos nucleos fíos fórmense, nun hai trescripción per parte de la ARN polimerasa II, de cuenta que los componentes proteicos formen nel so llugar un tapón perinucleolar.[39]
Speckles
editarN'ocasiones denominaos agrupaciones de gránulos intercromatínicos o compartimientos de factores de ayuste, los speckles, manches o llixos, son ricos en ARNnps procedentes del ayuste y otres proteínes del mesmu procesu que se precisen nel procesamientu del pre-ARNm.[40] Por cuenta de los requerimientos variables de la célula, la composición y llocalización d'estos cuerpos camuda d'alcuerdu a la trescripción de ARNm y a la regulación vía fosforilación de proteínes específiques.[41]
==== Cuerpos de dixebra Llamaos Cleavage bodies, n'inglés, suélense atopar acomuñaos a los cuerpos de Cajal, con un diámetru de 0,2 a 1,0 μm y en númberu de 1-10 por nucleu. A diferencia d'otros cuerpos nucleares, apaecen solamente mientres determinaos periodos del ciclu celular. Dalgunos d'estos contienen el complexu CPSF-100 (poles sos sigles n'inglés de cleavage and polyadenylation specificity factor: factor d'especificidá pa la corte y la poliadenilación), y pueden reparase predominantemente mientres les fases S y G, ente que los que contienen el factor de poliadenilación CstF-64-containing reparar principalmente na fase S. Tán acomuñaos col clúster de xenes de la histona.[42]
Cuerpos DDX1
editarLos cuerpos DDX1 son amestaos de la proteína DDX1, perteneciente a la familia d'helicases de ARN que contienen el motivu "DEAD box", atopar nun númberu que varia de dos a cuatro. Yá que paez qu'estos cuerpos son reclutados en llugares nos que se produció dañu nel ADN que ta hibridando con ADN, paez qu'estos cuerpos desempeñen un papel nel arreglu de zones con rotures de doble cadena, facilitando l'arreglu empuestu por patrón de rexones del xenoma transcripcionalmente actives.[42]
Función
editarLa principal función del nucleu celular ye controlar la espresión xenética y mediar na replicación del ADN mientres el ciclu celular. El nucleu apurre un allugamientu pa la trescripción na citoplasma, dexando niveles de regulación que nun tán disponibles en procariotas. Tien distintes funciones:
- Nel nucleu guarden los xenes en forma de cromosomes (mientres la mitosis) o cromatina (mientres la interfase)
- Entama los xenes en cromosomes lo que dexa la división celular
- Tresporta los factores de regulación al traviés de los poros nucleares
- Produz ácidu nucleico mensaxeru (ARNm) que codifica proteínes.
- Produz pre-ribosomas (ARNr) nel nucléolo.
Compartimentalización celular
editarLa envoltura nuclear dexa al nucleu controlar el so conteníu y dixebralo del restu de la citoplasma cuando sía necesariu. Esto ye importante pa controlar procesos en cualesquier de los llaos de la membrana nuclear. En dellos casos, cuando se precisa acutar un procesu citoplasmático, un participante clave retirar al nucleu, onde interactúa con factores de trescripción pa reprimir la producción de ciertes enzimes de la ruta. Esti mecanismu regulador tien llugar nel casu de la glucólisis, una ruta celular na que s'utiliza la glucosa pa producir enerxía. La hexoquinasa ye la enzima responsable del primer pasu de la glucólisis, produciendo glucosa-6-fosfatu a partir de la glucosa. A altes concentraciones de fructosa-6-fosfatu, una molécula que se forma darréu a partir de la glucosa-6-fosfatu, una proteína regulador retira la hexoquinasa al nucleu,[43] onde forma un complexu con otres proteínes nucleares que reprime la trescripción de los xenes implicaos na glucolisis.[44]
Pa controlar qué xenes se deben trescribir, la célula torga l'accesu físicu de dalgunos factores de trescripción responsables de regular la espresión xénica hasta que son activaos per otres rutes de señalización. Esto torga que se dean inclusive pequeños niveles d'espresión xénica desaparente. Por casu, nel casu de los xenes controlaos por NF-κB, que tán implicaos na mayor parte de les respuestes inflamatorias, la trescripción inducir en respuesta a una cascada de señalización celular como la que s'empecipia cola molécula señalizadora TNF-α xuniéndose a un receptor de la membrana celular, lo que produz el reclutamiento de proteínes señalizadoras y finalmente l'activación del factor de trescripción NF-κB. Una señal de llocalización nuclear que tien la proteína NF-κB déxa-y ser tresportada al traviés del poru nuclear al nucleu, onde aguiya la trescripción de los xenes diana.[6]
La compartimentalización dexa a la célula torgar la traducción de ARNm non ayustado.[45] El ARNm contién intrones que se deben retirar antes de ser traducíos pa producir proteínes funcionales. El ayuste efectuar nel interior del nucleu primero que el ARNm pueda aportar a los ribosomas pa la so traducción. Ensin el nucleu los ribosomas traduciríen ARNm recién trescritu y ensin procesar, lo que produciría proteínes mal plegaes y deformadas.
Espresión xénica
editarLa espresión xénica implica en primer llugar la trescripción, na que l'ADN utilízase como molde pa producir ARN. Nel casu de los xenes que codifican proteínes, el ARN xeneráu por esti procesu ye'l ARN mensaxeru (ARNm), que darréu precisa ser traducíu polos ribosomas pa formar una proteína. Yá que los ribosomas alcuéntrense fora del nucleu, el ARNm sintetizáu ten de ser esportáu.[46]
Yá que el nucleu ye'l llugar onde se da la trescripción, ta dotáu d'un conxuntu de proteínes que, o bien tán implicaes direutamente nesti procesu, o na so regulación. Ente éstes atopamos les helicases, que desenrollan la molécula d'ADN de doble cadena pa facilitar l'accesu de la maquinaria de síntesis, l'ARN polimerasa, que sintetiza'l ARN a partir del molde d'ADN, la topoisomerasa, que varia la cantidá de superenrollamiento del ADN, según una amplia variedá de factores de trescripción que regulen la espresión xénica.[47]
Procesamientu del pre-ARNm
editarLes molécules de ARNm acabante sintetizar conócense como trescritus primarios o pre-ARNm. Darréu débense someter a cambéu post-transcripcional nel nucleu antes de ser esportaos a la citoplasma. El ARNm qu'apaez nel nucleu ensin estos cambeos acaba degradáu en llugar d'utilizase pa la traducción nos ribosomas. Los trés cambeos principales son: La del estremu 5' (5' caping), la poliadenilación del estremu 3' y l'ayuste de ARN. Mientres permanez nel nucleu, el pre-ARNm acomuñóse con delles proteínes en complexos conocíos como ribonucleoproteínas heteroxénees nucleares o hnRNPs. La adición de los cambeos del estremu 5' tien llugar nel momentu de la trescripción y ye el primer pasu nos cambeos postranscripcionales. La cola de poliadenina 3' solo añader una vegada que la trescripción ta completa.
El ayuste (splicing o corte y empalme) de ARN, lleváu a cabu por un complexu denomináu espliceosoma ye'l procesu pol que los intrones retirar del pre-ARNm, permaneciendo namái los exones coneutaos pa formar una sola molécula continua. Esti procesu de normal remata tres los dos anteriores, pero puede empezar primero que la síntesis tea completa en trescritus con munchos exones.[5] Munchos pre-ARNm's, incluyendo los que codifican anticuerpos, pueden cortase y empalmar de múltiples formes pa producir distintes ARNm maduros, que por ello codifican distintes secuencies de proteínes. Esti procesu conozse como ayuste alternativu, y dexa la producción d'una gran variedá de proteínes a partir d'una cantidá llindada d'ADN.
Dinámica y regulación
editarTresporte nuclear
editarEl tresporte de molécules escontra l'esterior ya interior del nucleu, puede llevase a cabu gracies a qu'en toles célules eucariotes la envoltura nuclear ta furada por poros nucleares, constituyíos por grandes complexos multiproteicos. La entrada y salida de grandes molécules del nucleu ta puramente controlada polos complexos de poros nucleares. Anque les pequeñes molécules pueden entrar nel nucleu ensin regulación,[48] les macromolécules como'l ARN y les proteínes riquen acomuñar a carioferines llamaes importines pa entrar nel nucleu, y exportines pa salir. Les proteínes cargaes que tienen de ser translocadas dende la citoplasma al nucleu contienen curties secuencies d'aminoácidos conocíes como señales de llocalización nuclear que tán xuníes a les importinas, ente que les tresportaes dende'l nucleu a la citoplasma tienen señales d'esportación nuclear xuníes a les exportinas. La capacidá de les importinas y les exportinas pa tresportar la so carga ta regulada por GTPases, enzimes que hidrolizan GTP lliberando enerxía. La GTPasa clave nel tresporte nuclear ye Ran, que puede xunir o bien GTP o bien GDP (guanosina difosfato), dependiendo de si ta alcontrada nel nucleu o na citoplasma. Ente que les importinas dependen de Ran-GTP pa disociarse de la so carga, les exportinas precisen Ran-GTP pa xunise a la so carga.[12]
Señales de llocalización necesaries pal tresporte
editarLes señales de llocalización nuclear faen que'l fluxu de proteínes del citosol al nucleu sía selectivu. Estes señales namái tán presentes nes proteínes nucleares, consisten nuna secuencia curtia que va ente 4 y 8 aminoácido. Esta señal, cuando hai importación nuclear denominar señal de llocalización nuclear (NLS) y cuando hai esportación nuclear denominar señal d'esportación nuclear (NES).
Esisten dos tipos de NLS: les monopartitas y les bipartites. Les NLS monopartitas tán formaes por un namái grupu de residuos básiques y les NLS bipartites tán formaes por dos grupos de residuos de lisinas y argininas. Esti tipu de señales son reconocíes específicamente pola Importina α y les proteínes que les contienen son tresportaes al nucleu pol heterodímero Importina α/Importina β1. Per otru llau, les NES son secuencies curties d'aminoácidos hidrofóbicos, principalmente leucinas.
A estes señales de llocalización nuclear, que s'alcuentren nos poros nucleares, xúnense una o más nucleoporinas, que son proteínes citosólicas, que contienen la N-acetilglucosamina, un azucre simple qu'ayuda a la so identificación por aciu l'usu de lectinas y anticuerpo específicos. Les nucleoporinas collaboren dirixendo a la proteína nuclear escontra'l centru del complexu de poru, onde se xune a les fibrillas que tán estendíes escontra'l citosol y que se proyeuten a partir del aniellu del complexu. Estes fibrillas emponen a les proteínes nucleares escontra'l centru del complexu de poru, onde ye tresportada viviegamente escontra l'interior nuclear por aciu un procesu que rique la hidrólisis de GTP.
Carioferinas
editarSon proteínes mediadores del tresporte al traviés del complexu del poru nuclear. La so clasificación depende de la direición del tresporte pal que fueron primeramente descrites, clasificóse-yos como importinas y exportinas.
Les importinas, na so mayoría, pertenecen a la superfamilia de les importinas β y encárguense de regular el tresporte de la mayor parte de les proteínes y de distintes especies d'ARN, sacante ARNm.
Esportación nuclear
editarAsocede en condiciones d'alta concentración de Ran-GTP, reconoz una proteína que contién una NES (señal d'esportación nuclear) xunto a una molécula de Ran-GTP. El complexu ye entós capaz de interaccionar col complexu del poru nuclear y travesalo hasta la citoplasma. Una vegada ellí, otres proteínes Ran promueven l'actividá GTPasa de Ran, que hidroliza el GTP y pasa a convertise en Ran-GDP. La hidrólisis produz un cambéu conformacional en Ran, produciéndose'l desensamblaje de la exportina-carga, quedando la carga llibre na citoplasma. Les molécules de Ran-GDP y exportina reciclar pa un nuevu ciclu de tresporte.
Les proteínes especializaes d'esportación sirven pa la traslocación d'ARNm maduru y ARNt a la citoplasma dempués de que'l cambéu postranscripcional complétase. Esti mecanismu de control calidable ye importante debíu al papel central d'eses molécules na traducción de proteínes. La espresión desaparente d'una proteína por cuenta de una dixebra de exones incompleta o la incorporación impropia d'aminoácidos podría tener consecuencies negatives pa la célula. Por ello, el ARN non modificar por completu qu'algama la citoplasma ye degradáu en llugar de ser utilizáu na traducción.[5]
Importación nuclear
editarLa importación nuclear depende de que la importina s'una a la so carga nel citoplasma y tresportar al traviés del poru nuclear al nucleu. Les importinas interaccionan na citoplasma, en condiciones de baxa concentración de RanGTP, cola proteína con una NLS (señal de llocalización nuclear), y entra al interior del nucleu por aciu asociación con proteínes del complexu del poru nuclear. Una vegada nel nucleoplasma, la presencia d'altos niveles de RanGTP causa la destrucción del complexu importina-carga, lliberar la carga nel interior del nucleu. La Importina α ye tresportada de nuevu a la citoplasma por aciu la so interacción reiniciándose de nuevu'l procesu.
Regulación del tresporte ente'l nucleu y el citosol
editarEl tresporte ente'l citosol y el nucleu puede regulase inactivando la señal de llocalización nuclear de les proteínes nucleares por fosforilación o cuando diches proteínes xunir a proteínes citosólicas inhibidoras que les retienen nel citosol por aciu interacciones col citoesqueleto o con organelos específicos, o amazcaren les sos señales de llocalización nuclear. Sicasí, cuando la célula recibe l'estímulu necesariu, la proteína nuclear ye lliberada y ye tresportada escontra'l nucleu.
D'una forma similar, pue tar controlada la esportación d'ARN dende'l nucleu. Como na importación activa escontra'l nucleu, la esportación rique una señal. Ye probable que les señales d'esportación nuclear alcontrar nes subunidades proteiques de dichos complexos, y que s'activen dempués de ensamblarse correutamente colos componentes del ARN.
Por tou esto puede concluyise que'l mecanismu de tresporte de macromolécules al traviés del poru nuclear, ye bien distintu al mecanismu qu'asocede al traviés de les membranes d'otros organelos, pos el tresporte nuclear nun asocede por un tresportador proteicu que traviesa una o más bicapas lipídicas sinón por aciu un poru con una canal aguacienta reguláu. Tamién, ente que les proteínes nucleares son tresportaes al traviés de los poros calteniendo la so conformanza dafechu plegada, nel tresporte a otros organelos, les proteínes tienen qu'esplegase. A lo último, les señales de llocalización nuclear nun s'esanicien dempués del tresporte escontra'l nucleu, pos les proteínes nucleares han de ser importaes al nucleu delles vegaes, dempués de cada división celular. Pero, cuando una proteína foi importada a cualesquier otru organelo membranosu, el péptido señal ye de cutiu esaniciáu dempués de la translocación proteica.
Ensamblaxe y desensamblaje
editarMientres el so periodu de vida un nucleu puede desensamblarse, o bien nel intre de la división celular, o de resultes de l'apoptosis, una forma regulada de muerte celular. Mientres estos acontecimientos, los componentes estructurales del nucleu —la envoltura y la llámina— son sistemáticamente degradaos.
Mientres el ciclu celular la célula estremar pa formar dos célules. Por que ésti procesu sía posible, caúna de les nueves célules fía tien d'adquirir un xuegu completu de xenes, un procesu que rique la replicación de los cromosomes, según la segregación en xuegos separaos. Esto produzse cuando los cromosomes yá retrucaos, les cromátides fíes, xunir a los microtúbulos, que de la mesma xunir a distintos centrosomes. Les cromátides fía pueden ser fraccionaes escontra llocalizaciones separaes na célula. Sicasí, en munches célules el centrosoma alcontrar na citoplasma, fora del nucleu, polo que los microtúbulos seríen incapaces de xunise a les cromátides en presencia de la envoltura nuclear.[49] Por tanto, nos estadios tempranos del ciclu celular, empezando en profase y hasta casi la prometafase, desmantélase la membrana nuclear.[15] De forma similar, mientres el mesmu periodu se desensambla la llámina nuclear, un procesu que ta reguláu pola fosforilación de les llámines.[50] Escontra'l final del ciclu celular refórmase la membrana nuclear, y en redol coles mesmes, la llámina nuclear se reensambla desfosforilando les proteínes llaminares.[50]
L'apoptosis ye un procesu controláu nel que los componentes estructurales de la célula son destruyíos, lo que produz la muerte de la célula. Los cambeos acomuñaos cola apóptosis afecten direutamente al nucleu y a los sos conteníos, por casu na condensación de la cromatina y la desintegración de la envoltura nuclear y la llámina. La destrucción de les redes de llámina ta controlada por proteases apoptóticas especializaes denominaes caspases, que desintegran la llámina nuclear y de esa manera degraden la integridá estructural del nucleu. La desintegración de la llámina nuclear utilizar n'ocasiones nos llaboratorios como indicador de l'actividá de la caspasa n'ensayos d'actividá apoptótica temprana.[15] Les célules qu'espresen llámines resistentes a les caspasas son deficientes nos cambeos nucleares rellacionaos cola apoptosis, lo que suxure que les llámines desempeñen un papel importante nel entamu de los eventos que conducen a la degradación apoptótica del nucleu.[15] La inhibición del propiu ensamblaxe de la llámina nuclear ye por sigo mesma un inductor de la apoptosis.[51]
La envoltura nuclear actúa como una barrera qu'evita que virus d'ADN o ARN enfusen nel nucleu. Dellos virus precisen aportar a proteínes dientro del nucleu pa retrucar o ensamblarse. Los virus d'ADN, como'l herpesvirus retrúquense y ensamblan nel nucleu celular, y salen brotando al traviés de la membrana nuclear interna. Esti procesu acompañar del desensamblaje de la llámina nuclear na cara nuclear de la membrana interna.[15]
Célules anucleadas y polinucleadas
editarAnque la mayor parte de les célules tienen un únicu nucleu, dellos tipos celulares escarecen d'él, en cuantes qu'otros tienen múltiples nucleos. Esto pue ser un procesu normal, como ye nel casu de la maduración de los eritrocitos, o bien la resultancia d'una división celular defectuosa.
Les célules anucleadas escarecen de nucleu, y por lo mesmo son incapaces d'estremase pa producir célules fíes. El casu meyor conocíu de célula anucleada ye'l eritrocitu de mamíferu, que tamién escarez d'otros orgánulos como mitocondries, y sirven en principiu como vehículos de tresporte d'osíxenu dende los pulmones a los texíos. Los eritrocitos maurecen gracies a la eritropoyesis na migollu oseu, onde pierden el so nucleu, orgánulos y ribosomas. El nucleu ye espulsáu mientres el procesu de diferenciación d'eritroblasto a reticulocito, que ye'l precursor inmediatu del eritrocitu maduru.[52] mutágenos puede inducir la lliberación de dellos eritrocitos inmaduros "micronucleados" a la riega sanguínea.[53][54] Tamién pueden apaecer célules anucleadas a partir d'una división celular defectuosa na qu'una célula fía escarez de nucleu, ente que la otra tien dos.
Les célules polinucleadas contienen múltiples nucleos. La mayor parte de los protozoos de la clase Acantharea,[55] y dalgunos fungos que formen micorrices,[56] tienen célules polinucleadas de forma natural. Otros exemplos seríen los parásitos intestinales del xéneru Giardia, que tien dos nucleos en cada célula.[57] Nos seres humanos, el músculu esqueléticu tien célules, llamaes miocitos, que se converten en polinucleadas mientres el so desenvolvimientu. La disposición resultante de los nucleos na rexón periférica de la célula dexa un espaciu intracelular máximu pa les miofibrilles.[5] Les célules multinucleadas tamién pueden ser anormales n'humanos. Por casu, les que surden de la fusión de monocitos y macrófagos, conocíes como célules multinucleadas xigantes, pueden ser reparaes n'ocasiones acompañando a la inflamación,[58] y tamién tán implicaes na formación de tumores.[59]
Evolución
editarAl ser la meyor carauterística que define la célula eucariota, l'orixe evolutivu del nucleu foi oxetu de muncha especulación. Ente les teoríes propuestes, pueden considerase cuatro comos les principales, anque nenguna d'elles atopó un ampliu sofitu.[60]
Teoríes endosimbioticas
editarLa teoría conocida como "modelu sintrófico" propón qu'una rellación simbiótica ente arquies y bacteries creó la primer célula eucariota nucleada. Establezse la hipótesis de que la simbiosis tuvo llugar cuando una arquia antigua similar a los actuales metanógenos fueron invadíos y parasitados por bacteries similares a les actuales myxobacteria, formando eventualmente el nucleu primitivu. Esta teoría ye análoga a teoría aceptada del orixe de les mitocondries y cloroplastos eucariotes, de los que se piensa que se desenvolvieron por una rellación endosimbionte similar ente protoeucariotas y bacteries aerobies.[61] L'orixe arqueano del nucleu ta sofitáu pola circunstancia de que tanto arquies como eucariotes tienen xenes similares en ciertes proteínes, incluyendo les histones. Al reparar que les myxobacterias son móviles, pueden formar complexos multicelulares y tienen proteínes G similares a les d'eucariotes, tamién puede aceptase un orixe bacterianu de la célula eucariota.[62] Una propuesta similar establez qu'una célula similar al eucariota, el cronocito, apaeció de primeres, y darréu fagocitó arquies y bacteries pa dar llugar al nucleu y a la célula eucariota.[63]
Un modelu más revesosu, conocíu como eucariogénesis viral afirma que munches traces de la célula eucariota como la presencia d'un nucleu que se sigue cola membrana surdieron pola infeición d'un antepasáu procariota por un gran virus d'ADN (posiblemente d'un Virus nucleocitoplasmáticos d'ADN de gran tamañu). Esto ta suxuríu sobre la base de semeyances ente eucariotes y virus como les hebras lliniales d'ADN, el procesamientu "caping" del estremu 5' del ARNm y la fuerte unión a proteínes del ADN (faciendo a les histonas análogues de la envoltura vírica). Una versión d'esta propuesta suxure que'l nucleu evolucionó concertadamente cola fagocitosis pa dar llugar a un depredador celular primitivu.[64] Otra variante propón que los eucariotes aniciar d'arquies primitives infestaes por poxvirus, basándose na semeyanza de les modernes ADN polimerasas ente éstos y los eucariotes.[65][66] Suxurióse que la cuestión ensin resolver de la evolución de la sexualidá pudo tar rellacionada cola hipótesis de la eucariogénesis viral.[67]
Teoríes non endosimbioticas
editarEsti modelu propón que les célules protoeucariotas evolucionaron a partir de bacteries ensin que se diera un estadiu simbionte. Esti modelu basar na esistencia d'una bacteria moderna perteneciente al filu de les planctomycetes que tienen una estructura nuclear con poros primitivos y otres estructures compartimentalizadas por membrana.[68]
Finalmente, una propuesta bien recién suxure que les variantes tradicionales de les teoríes endosimbiontes son insuficientes pa esplicar l'orixe del nucleu eucariota. Esti modelu, denomináu la hipótesis de la exomembrana, suxure que'l nucleu aniciar en llugar d'ello a partir d'una célula ancestral orixinal que desenvolvió una segunda membrana celular esterior. La membrana interior que zarraba la célula orixinal convirtióse entós na membrana nuclear evolucionando pa desenvolver estructures de poru cada vez más ellaboraes pal pasu de componentes celulares sintetizaos internamente, como les subunidades ribosómicas.[69]
Referencies
editar- ↑ Leeuwenhoek, A. van: Opera Omnia, seu Arcana Naturae ope exactissimorum Microscopiorum detecta, experimentis variis comprobata, Epistolis ad dellos illustres viros. J. Arnold et Delphis, A. Beman, Lugdinum Batavorum 1719–1730. Citáu por: Dieter Gerlach, Geschichte der Mikroskopie. Verlag Harry Deutsch, Frankfurt am Main, Germany, 2009. ISBN 978-3-8171-1781-9.
- ↑ Harris, H (1999). The Birth of the Cell. New Haven: Yale University Press.
- ↑ Brown, Robert (1866). «On the Organs and Mode of Fecundation of Orchidex and Asclepiadea». Miscellaneous Botanical Works I: páxs. 511–514.
- ↑ 4,0 4,1 Cremer, Thomas (1985). Von der Zellenlehre zur Chromosomentheorie. Berlin, Heidelberg, New York, Tokyo: Springer Verlag. ISBN 3-540-13987-7. Online Version here
- ↑ 5,0 5,1 5,2 5,3 5,4 5,5 5,6 5,7 Lodish, H; Berk A, Matsudaira P, Kaiser CA, Krieger M, Scott MP, Zipursky SL, Darnell J. (2004). Molecular Cell Biology, 5th, New York: WH Freeman.
- ↑ 6,0 6,1 6,2 6,3 (2002) Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, Peter Walter: Molecular Biology of the Cell, Chapter 4, pages 191-234, 4th, Garland Science.
- ↑ González, A.M. Nucleu. Morfoloxía de Plantes Vasculares. Facultá de Ciencies Agraries, Universidá Nacional del Nordeste. Consultáu'l 30 d'ochobre de 2009.
- ↑ Clegg JS (febreru 1984). «Properties and metabolism of the aqueous cytoplasm and its boundaries». Am. J. Physiol. 246 (2 Pt 2): páxs. R133–51. PMID 6364846. http://ajpregu.physiology.org/cgi/pmidlookup?view=reprint&pmid=6364846.
- ↑ Paine P, Moore L, Horowitz S (1975). «Nuclear envelope permeability». Nature 254 (5496): páxs. 109–114. doi:. PMID 1117994.
- ↑ (1996) «Ch3», Rodney Rhoades, Richard Pflanzer: Human Physiology, 3rd, Saunders College Publishing.
- ↑ Shulga N, Mosammaparast N, Wozniak R, Goldfarb D (2000). «Yeast nucleoporins involved in passive nuclear envelope permeability». J Cell Biol 149 (5): páxs. 1027–1038. doi:. PMID 10831607.
- ↑ 12,0 12,1 Pemberton L, Paschal B (2005). «Mechanisms of receptor-mediated nuclear import and nuclear export». Traffic 6 (3): páxs. 187–198. doi:. PMID 15702987.
- ↑ Stuurman N, Heins S, Aebi O (1998). «Nuclear lamins: their structure, assembly, and interactions». J Struct Biol 122 (1–2): páxs. 42–66. doi:. PMID 9724605.
- ↑ Goldman A, Moir R, Montag-Lowy M, Stewart M, Goldman R (1992). «Pathway of incorporation of microinjected lamin A into the nuclear envelope». J Cell Biol 119 (4): páxs. 725–735. doi:. PMID 1429833.
- ↑ 15,0 15,1 15,2 15,3 15,4 Goldman R, Gruenbaum Y, Moir R, Shumaker D, Spann T (2002). «Nuclear lamins: building blocks of nuclear architecture». Gen Dev 16 (5): páxs. 533–547. doi:. PMID 11877373. http://www.genesdev.org/cgi/content/full/16/5/533.
- ↑ Moir RD, Yoona M, Khuona S, Goldman RD. (2000). «Nuclear Lamins A and B1: Different Pathways of Assembly during Nuclear Envelope Formation in Living Cells». Journal of Cell Biology 151 (6): páxs. 1155–1168. doi:. PMID 11121432.
- ↑ «Alteration of nuclear lamin organization inhibits RNA polymerase II–dependent transcription». Journal of Cell Biology 156 (4): páxs. 603–608. 2002. doi:. PMID 11854306.
- ↑ Mounkes LC, Stewart CL (2004). «Aging and nuclear organization: lamins and progeria». Current Opinion in Cell Biology 16: páxs. 322–327. doi:. PMID 15145358.
- ↑ Ehrenhofer-Murray A (2004). «Chromatin dynamics at DNA replication, transcription and repair». Eur J Biochem 271 (12): páxs. 2335–2349. doi:. PMID 15182349.
- ↑ Grigoryev S, Bulynko Y, Popova Y (2006). «The end adjusts the means: heterochromatin remodelling during terminal cell differentiation». Chromosome Res 14 (1): páxs. 53–69. doi:. PMID 16506096.
- ↑ Schardin, Margit; T. Cremer, H. D. Hager, M. Lang (avientu 1985). «Specific staining of human chromosomes in Chinese hamster x man hybrid cell lines demonstrates interphase chromosome territories». Human Genetics (Springer Berlin / Heidelberg) 71 (4): páxs. 281–287. doi:. PMID 2416668. http://www.springerlink.com/content/lv101t8w17306071/.
- ↑ Lamond, Angus I.; William C. Earnshaw (24 d'abril de 1998). «Structure and Function in the Nucleus». Science 280: páxs. 547–553. doi:. PMID 9554838.
- ↑ Kurz, A; S Lampel, JE Nickolenko, J Bradl, A Benner, RM Zirbel, T Cremer and P Lichter (1996). «Active and inactive xenes localize preferentially in the periphery of chromosome territories». The Journal of Cell Biology (The Rockefeller University Press) 135: p. 1195–1205. doi:. PMID 8947544. http://intl.jcb.org/cgi/content/abstract/135/5/1195.
- ↑ NF Rothfield, BD Stollar (1967). «The Relation of Immunoglobulin Class, Pattern of Antinuclear Antibody, and Complement-Fixing Antibodies to DNA in Sera from Patients with Systemic Lupus Erythematosus». J Clin Invest 46 (11): páxs. 1785–1794. PMID 4168731.
- ↑ S Barned, AD Goodman, DH Mattson (1995). «Frequency of anti-nuclear antibodies in multiple sclerosis». Neurology 45 (2): páxs. 384–385. PMID 7854544.
- ↑ Hernandez-Verdun, Daniele (2006). «Nucleolus: from structure to dynamic». Histochem. Cell. Biol 125 (125): páxs. 127–137. doi:.
- ↑ 27,0 27,1 Lamond, Angus I.; Judith Y. Sleeman. «Nuclear substructure and dynamics». Current Biology 13 (21): páxs. R825–828. doi:. PMID 14588256.
- ↑ 28,0 28,1 28,2 Cioce M, Lamond A. «Cajal bodies: a long history of discovery». Annu Rev Cell Dev Biol 21: p. 105–131. doi:. PMID 16212489.
- ↑ 29,0 29,1 29,2 Pollard, Thomas D.; William C. Earnshaw (2004). Cell Biology. Philadelphia: Saunders. ISBN 0-7216-3360-9.
- ↑ 30,0 30,1 30,2 Dundr, Miroslav; Tom Misteli (2001). «Functional architecture in the cell nucleus». Biochem. J. (356): páxs. 297–310. doi:. PMID 11368755.
- ↑ Plantía:Cita entrevista
- ↑ Goebel, H.H.; I Warlow (xineru 1997). «Nemaline myopathy with intranuclear rods—intranuclear rod myopathy». Neuromuscular Disorders 7 (1): páxs. 13–19. doi:. PMID 9132135.
- ↑ 33,0 33,1 33,2 Matera AG, Frey MA. (1998). «Coiled Bodies and Gems: Janus or Gemini?». American Journal of Human Genetics 63 (2): páxs. 317–321. doi:. PMID 9683623.
- ↑ Matera, A. Gregory (1998). «Of Coiled Bodies, Gems, and Salmon». Journal of Cellular Biochemistry (70): páxs. 181–192. doi:. PMID 9671224.
- ↑ Saunders WS, Cooke CA, Earnshaw WC (1991). «Compartmentalization within the nucleus: discovery of a novel subnuclear region.». Journal of Cellular Biology 115 (4): páxs. 919–931. doi:. PMID 1955462
- ↑ Pombo A, Cuello P, Schul W, Yoon J, Roeder R, Cook P, Murphy S (1998). «Rexonal and temporal specialization in the nucleus: a transcriptionally active nuclear domain rich in PTF, Oct1 and PIKA antigens associates with specific chromosomes early in the cell cycle». EMBO J 17 (6): páxs. 1768–1778. doi:. PMID 9501098.
- ↑ 37,0 37,1 Fox, Archa et al. (2002). «Paraspeckles:A Novel Nuclear Domain». Current Biology 12: páxs. 13–25. doi:. http://www.current-biology.com/content/article/abstract?uid=PIIS0960982201006327.
- ↑ 38,0 38,1 Fox, Archa; Wendy Bickmore. «Nuclear Compartments: Paraspeckles». Nuclear Protein Database. Consultáu'l 6 de marzu de 2007.
- ↑ 39,0 39,1 Fox, A. et al. (2005). «P54nrb Forms a Heterodimer with PSP1 That Localizes to Paraspeckles in an RNA-dependent Manner». Molecular Biology of the Cell 16: páxs. 5304–5315. doi:. PMID 16148043. http://www.molbiolcell.org/cgi/reprint/16/11/5304. PMID 16148043
- ↑ Lamond AI, Spector DL (agostu 2003). «Nuclear speckles: a model for nuclear organelles». Nat. Rev. Mol. Cell Biol. 4 (8): páxs. 605–12. doi:. PMID 12923522.
- ↑ Handwerger, Korie Y.; Joseph G. Gall (xineru 2006). «Subnuclear organelles: new insights into form and function». TRENDS in Cell Biology 16 (1): páxs. 19–26. doi:. PMID 16325406.
- ↑ 42,0 42,1 Li, L; Roy K, Katyal S, Sun X, Bléoo S, Godbout R. (marzu 2006). «Dynamic nature of cleavage bodies and their spatial relationship to DDX1 bodies, Cajal bodies, and gems». Mol Biol Cell 17 (3): páxs. 1126-40. doi:. PMID 16371507. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC1382303/?tool=pubmed.
- ↑ Lehninger, Albert L.; David L. Nelson, Michael M. Cox. (2000). Lehninger principles of biochemistry, 3rd, New York: Worth Publishers. ISBN 1-57259-931-6.
- ↑ Moreno F, Ahuatzi D, Riera A, Palomino CA, Herrero P. (2005). «Glucose sensing through the Hxk2-dependent signalling pathway.». Biochem Soc Trans 33 (1): páxs. 265–268. doi:. PMID 15667322. PMID 15667322
- ↑ Görlich, Dirk; Ulrike Kutay (1999). «Transport between the cell nucleus and the cytoplasm». Ann. Rev. Cell Dev. Biol. (15): páxs. 607–660. doi:. PMID 10611974.
- ↑ Nierhaus, Knud H.; Daniel N. Wilson (2004). Protein Synthesis and Ribosome Structure: Translating the Genome. Wiley-VCH. ISBN 3527306382.
- ↑ Nicolini, Claudio A. (1997). Genome Structure and Function: From Chromosomes Characterization to Xenes Technology. Springer. ISBN 0792345657.
- ↑ Watson, JD; Baker TA, Bell SP, Gann A, Levine M, Losick R. (2004). «Ch9–10», Molecular Biology of the Gene, 5th, Peason Benjamin Cummings; CSHL Press..
- ↑ Lippincott-Schwartz, Jennifer (7 de marzu de 2002). «Cell biology: Ripping up the nuclear envelope». Nature 416 (6876): páxs. 31–32. doi:. PMID 11882878.
- ↑ 50,0 50,1 Boulikas T (1995). «Phosphorylation of transcription factors and control of the cell cycle». Crit Rev Eukaryot Gene Expr 5 (1): páxs. 1–77. PMID 7549180.
- ↑ Steen R, Collas P (2001). «Mistargeting of B-type lamins at the end of mitosis: implications on cell survival and regulation of lamins A/C expression». J Cell Biol 153 (3): páxs. 621–626. doi:. PMID 11331311.
- ↑ Skutelsky, Y.; Danon D. (xunu 1970). «Comparative study of nuclear expulsion from the late erythroblast and cytokinesis». J Cell Biol (60(3)): páxs. 625–635. doi:. PMID 5422968.
- ↑ Torous, DK; Dertinger SD, Hall NE, Tometsko CR. (2000). «Enumeration of micronucleated reticulocytes in rat peripheral blood: a flow cytometric study». Mutat Res (465(1–2)): páxs. 91–99. doi:. PMID 10708974.
- ↑ Hutter, KJ; Stohr M. (1982). «Rapid detection of mutagen induced micronucleated erythrocytes by flow cytometry». Histochemistry (75(3)): páxs. 353–362. doi:. PMID 7141888.
- ↑ Zettler, EL coautores =Sogin ML, Caron DA (1997). «Phylogenetic relationships between the Acantharea and the Polycystinea: A molecular perspective on Haeckel's Radiolaria». Proc Natl Acad Sci USA (94): páxs. 11411–11416. doi:. PMID 9326623.
- ↑ Horton, TR (2006). «The number of nuclei in basidiospores of 63 species of ectomycorrhizal Homobasidiomycetes». Mycologia (98(2)): páxs. 233–238. doi:. PMID 16894968.
- ↑ Adam RD (avientu 1991). «The biology of Giardia spp». Microbiol. Rev. 55 (4): páxs. 706–32. PMID 1779932. PMC 372844. http://mmbr.asm.org/cgi/pmidlookup?view=long&pmid=1779932.
- ↑ McInnes, A; Rennick DM (1988). «Interleukin 4 induces cultured monocytes/macrophages to form giant multinucleated cells». J Exp Med (167): páxs. 598–611. doi:. PMID 3258008.
- ↑ Goldring, SR; Roelke MS, Petrison KK, Bhan AK (1987). «Human giant cell tumors of bone identification and characterization of cell types». J Clin Invest (79(2)): páxs. 483–491. doi:. PMID 3027126.
- ↑ Pennisi Y. (2004). «Evolutionary biology. The birth of the nucleus». Science 305 (5685): páxs. 766–768. doi:. PMID 15297641.
- ↑ Margulis, Lynn (1981). Symbiosis in Cell Evolution. San Francisco: W. H. Freeman and Company, páx. 206–227. ISBN 0-7167-1256-3.
- ↑ Lopez-Garcia P, Moreira D. (2006). «Selective forces for the origin of the eukaryotic nucleus». Bioessays 28 (5): páxs. 525–533. doi:. PMID 16615090.
- ↑ Hartman H, Fedorov A. (2002). «The origin of the eukaryotic cell: a genomic investigation». Proc Natl Acad Sci U S A. 99 (3): páxs. 1420–1425. doi:. PMID 11805300.
- ↑ Bell PJ. (2001). "Viral eukaryogenesis: was the ancestor of the nucleus a complex DNA virus?" J Mol Biol Sep;53(3):251–256. PMID 11523012
- ↑ Takemura M. (2001). Poxviruses and the origin of the eukaryotic nucleus. J Mol Evol 52(5):419–425. PMID 11443345
- ↑ Villarreal L, DeFilippis V (2000). «A hypothesis for DNA viruses as the origin of eukaryotic replication proteins». J Virol 74 (15): páxs. 7079–7084. doi:. PMID 10888648.
- ↑ Bell PJ (7 de payares de 2006). «Sex and the eukaryotic cell cycle is consistent with a viral ancestry for the eukaryotic nucleus». J Theor Biol 243 (1): páxs. 54–63. PMID 16846615.
- ↑ Fuerst JA. (2005). «Intracellular compartmentation in planctomycetes». Annu Rev Microbiol. 59: p. 299–328. doi:. PMID 15910279.
- ↑ de Roos AD (2006). «The origin of the eukaryotic cell based on conservation of existing interfaces». Artif Life 12 (4): páxs. 513–523. doi:. PMID 16953783.
Enllaces esternos
editar